13:19 . 03.07 .. terceiro dia do mês, eu no momento estou no computador da faculdade e nem sei se podia estar postando nada disso, estou morrendo de sono, ontem diferente de tantas outras vezes pensei: vou sair e pronto. e saí, daí estou meio dãan. Bem vou ignorar tudo isso e começar a tentar trabalhar em algo útil aqui. e o conteúdo de hoje começa especificamente em Bases estequiométricas e começaremos a discutir a lei dos gases, daí darei continuidade em outras coisas que me pareci útil, enfim...
- Uma daquelas coisas que todos temos que saber, assim como nos e essencial aprender a andar , a falar, a conversar.. ou seja, daquelas coisas que e agora e vai ter que ser comecaremos a falar sobre Lavoisier, todos quando passamos pelo ensino medio ouvimos falar de m cara muito famoso, chamado Lavoisier, ou no minimo todos deveriamos ter ouvido falar, esse cara fez uma lei que leva o seu nome chamada: Lei da conservação da massa ou lei da conservacao da materia.
- Lavosier fez inumeras exeriencias, nas quais pesava as substancias participantes, antes e depois da reacao, verificando entao que a massa total do sistema permanecia inalterado quando a reacao ocorria em um sistema fechado. Com base nessas experiencias, Lavoisier enunciou, em 1774, a seguinte lei: Numa reacao quimica, a soma das massas dos reagente e igual a soma das massas dos produtos.
- Sejam mA, mB , mC e mD as massas das substancias A, B, C e D, participantes de uma reacao expressa pela equacao:
- A + B -> C + D
- de acordo com a lei de Lavoisier: mA + mB = mC + mD
- A lei de Lavoisier e frequentemente enunciada de uma maneira bem simplies " Na natureza nada se cria e nada se perde".
A equação que descreve a relação entre pressão, volume, temperatura e quantidade- (em mols) de gases, denominada EQUAÇÃO DE ESTADO, é a seguinte:

onde:
 = Pressão
= Pressão = Volume
= Volume = Moles de gás.
= Moles de gás.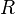 = Constante universal dos Gases Perfeitos
= Constante universal dos Gases Perfeitos = Temperatura em Kelvin.
= Temperatura em Kelvin.
daqui a pouco continuo..











